
近日,我校生物治疗国家重点实验室董浩浩研究员团队在国际期刊 Nature Communications(影响因子11.878)上发表了题为“Cryo-EM structures of lipopolysaccharide transporter LptB2FGC in lipopolysaccharide or AMP-PNP-bound states reveal its transport mechanism”的研究论文。该研究主要工作由董浩浩研究员团队与浙江大学医学院冷冻电镜中心主任张兴教授团队合作完成。论文第一作者为我校生物治疗国家重点实验室副教授唐晓迪博士,浙江大学冷冻电镜中心工程师常圣海博士,我校博士研究生罗庆华及武汉大学药学院张郑宇研究员为并列第一作者。我校生物治疗国家重点实验室/国家老年疾病临床医学研究中心为该论文第一作者单位和通讯作者单位。
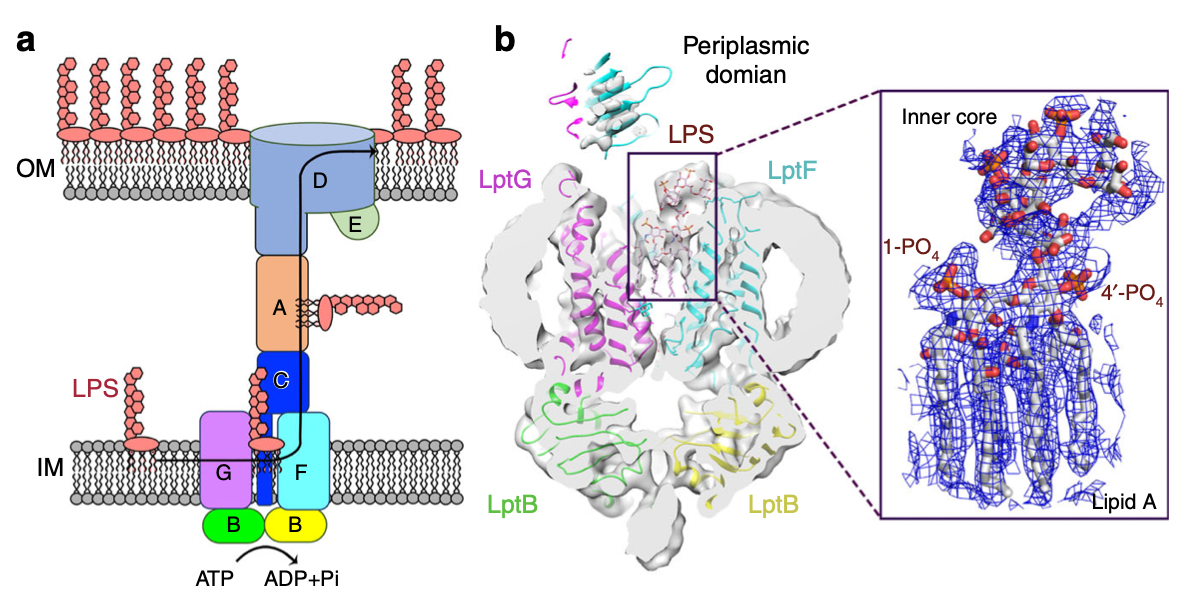
该研究揭示多重耐药细菌-革兰氏阴性菌用于转运外膜脂多糖的蛋白质机器复合物LptB2FGC,与其底物脂多糖或AMP-PNP结合状态下的高分辨率冷冻电镜结构。通过对结构的分析和细胞体内功能的研究,揭示该蛋白质机器的重要功能位点及其高效能的转运机制。
目前多重耐药细菌或“超级细菌”的感染已给人类健康带来重大威胁。世界卫生组织(WHO)对新型抗生素的迫切需求程度分成了三大类别:中等重要、十分重要和极为重要,其中针对铜绿假单胞菌、肠杆菌和鲍曼不动杆菌的三种革兰氏阴性细菌的新型抗生素的研发被列为极为重要。革兰氏阴性菌其特有的外膜结构-脂多糖保护层是其耐药的重要原因,因此,破坏外膜脂多糖的合成和转运是研究新型抗菌素的重要途径。本课题研究的目标蛋白质机器LptB2FGC在革兰氏阴性菌负责将外膜主要成分脂多糖从内膜转运到外膜。该复合体在细菌内膜和外膜之间形成转运通道,将外膜脂多糖分子从细菌内膜外小叶中抽提并通过ATP结合(非水解)引发核苷酸结合域(NBDs)与跨膜结构域(TMDs)的蛋白肽链的构型变化,从而将脂多糖从底物结合腔挤压到周质域(PDs)中去,最终被周质蛋白传送到外膜,形成具有耐药作用的保护层。研究揭示了LptB2FGC对脂多糖的识别与转运的机理,并表明位于NBDs和TMDs界面的两个精氨酸环在转运中起到重要的构象交流功能。本研究通过突变确定了多个可引发细菌死亡的参与复合物转运的功能位点。因此,这些功能位点可作为新型抗菌素设计的有效靶点。该研究对抵抗超级细菌感染的新型药物研发具有重要意义。